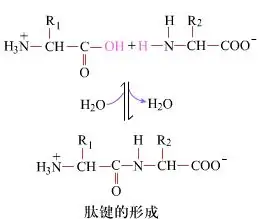
Sa ibabaw, ang pagbuo ng mga peptide bond, na nagbubunga ng dipeptides, ay isang simpleng proseso ng kemikal.Nangangahulugan ito na ang dalawang bahagi ng amino acid ay pinag-uugnay ng isang peptide bond, isang amide bond, habang inaalis ang tubig.
Ang pagbuo ng peptide bond ay ang pag-activate ng isang amino acid sa ilalim ng banayad na mga kondisyon ng reaksyon.(A) carboxyl moiety, pangalawang amino acid (B) Ang nucleophilic activated carboxyl moiety pagkatapos ay bumubuo ng dipeptide (AB)."Kung ang carboxyl component (A) ay hindi protektado, ang pagbuo ng peptide bond ay hindi makokontrol."Ang mga by-product tulad ng linear at cyclic peptides ay maaaring ihalo sa mga target compound AB.Samakatuwid, ang lahat ng mga functional na grupo na hindi kasangkot sa pagbuo ng peptide bond ay dapat na protektahan sa isang pansamantalang nababaligtad na paraan sa panahon ng peptide synthesis.
Kaya, ang peptide synthesis - ang pagbuo ng bawat peptide bond - ay nagsasangkot ng tatlong hakbang ng pagsasama-sama.
Ang unang hakbang ay ang paghahanda ng ilang amino acid na nangangailangan ng proteksyon, at ang zwitterionic na istraktura ng mga amino acid ay wala na.
Ang ikalawang hakbang ay isang dalawang-hakbang na reaksyon upang bumuo ng mga peptide bond, kung saan ang carboxyl group ng N-protected amino acid ay unang naisaaktibo sa aktibong intermediate at pagkatapos ay nabuo ang peptide bond.Ang pinagsamang reaksyong ito ay maaaring mangyari alinman bilang isang hakbang na reaksyon o bilang dalawang sunud-sunod na reaksyon.
Ang ikatlong hakbang ay ang pumipili na pag-alis o kumpletong pag-alis ng proteksiyon na base.Bagama't ang lahat ng pag-aalis ay maaari lamang mangyari pagkatapos ma-assemble ang lahat ng peptide chain, kailangan din ang piling pag-alis ng mga pangkat na proteksiyon upang maipagpatuloy ang synthesis ng peptide.
Dahil ang 10 amino acids (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec at Cys) ay naglalaman ng mga side chain functional group, na nangangailangan ng selective na proteksyon, na ginagawang mas kumplikado ang peptide synthesis.Ang pansamantala at semi-permanenteng mga base ng proteksyon ay dapat na makilala dahil sa iba't ibang mga kinakailangan para sa pagpili.Ang mga pansamantalang grupo ng proteksyon ay ginagamit sa susunod na hakbang upang ipakita ang pansamantalang proteksyon ng amino acid o carboxyl functional group.Ang mga semi-permanent na grupong proteksiyon ay tinanggal nang hindi nakakasagabal sa nabuo nang mga peptide bond o amino acid side chain, minsan sa panahon ng synthesis.
"Sa isip, ang activation ng carboxyl component at ang kasunod na pagbuo ng peptide bonds (coupling reactions) ay dapat na mabilis, nang walang racemic o by-product formation, at ang mga molar reactant ay dapat ilapat upang makamit ang mataas na ani."Sa kasamaang palad, wala sa mga pamamaraan ng pagsasama ng kemikal ang nakakatugon sa mga kinakailangang ito, at kakaunti ang angkop para sa praktikal na synthesis.
Sa panahon ng peptide synthesis, ang mga functional na grupo na kasangkot sa iba't ibang mga reaksyon ay karaniwang naka-link sa manual center, ang glycine ang tanging pagbubukod, at may potensyal na panganib ng pag-ikot.
Ang huling hakbang sa siklo ng synthesis ng peptide ay ang pag-alis ng lahat ng mga pangkat na proteksiyon.Ang piling pag-alis ng mga pangkat na proteksiyon ay mahalaga para sa extension ng chain ng peptide bilang karagdagan sa kinakailangan para sa kumpletong pag-alis ng proteksyon sa synthesis ng dipeptide.Ang mga sintetikong estratehiya ay dapat na maingat na pinaplano.Depende sa madiskarteng pagpili, maaaring piliing alisin ng N ang mga grupong nagpoprotekta sa α-amino o carboxyl.Ang terminong "diskarte" ay tumutukoy sa pagkakasunud-sunod ng mga reaksyon ng condensation ng mga indibidwal na amino acid.Sa pangkalahatan, may pagkakaiba sa pagitan ng unti-unting synthesis at fragment condensation.Ang peptide synthesis (kilala rin bilang "conventional synthesis") ay nagaganap sa solusyon.Sa karamihan ng mga kaso, ang unti-unting pagpapahaba ng peptide chain ay maaari lamang ma-synthesize sa pamamagitan ng paggamit ng peptide chain upang mag-synthesize ng mas maiikling mga fragment.Upang ma-synthesize ang mas mahabang peptides, ang mga target na molekula ay dapat na hatiin sa naaangkop na mga fragment at matukoy na maaari nilang i-minimize ang antas ng pagkita ng kaibhan sa C terminus.Matapos unti-unting tipunin ang mga indibidwal na fragment, pagsasamahin ang target na tambalan.Kasama sa diskarte ng peptide synthesis ang pagpili ng pinakamahusay at pinakaangkop na proteksiyon na fragment, at ang diskarte ng peptide synthesis ay kinabibilangan ng pagpili ng pinakaangkop na kumbinasyon ng mga proteksiyon na base at ang pinakamahusay na paraan ng fragment conjugation.
Oras ng post: Hul-19-2023